Si
Por qué lo más común es que
se dé entre bacterias de las mismas especies.
En los últimos años se ha
logrado desarrollar sistemas artificiales para producir “células competentes”
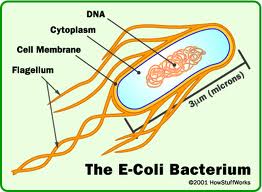
en algunas de ellas (como Escherichia coli, Salmonella typhimurium y algunas especies de Pseudomonas), lo cual ha
hecho avanzar los estudios genéticos, especialmente mediante manipulaciones in
vitro: por ejemplo, la transformación artificial de E. coli con ADN plasmídico
es una de los métodos básicos de la Ingeniería Genética.
La transformación es la transferencia genética
que resulta de la incorporación de DNA desnudo por una célula receptora desde
una célula donadora.
Ciertas bacterias (ej.
Bacillus, Haemophilus, Neisseria, Pneumococcus) son capaces de tomar DNA del
medio ambiente y ese DNA que es introducido puede llegar a ser incorporado al
cromosoma de la célula bacteriana receptora. Esto se llama transformación
natural. Porqué si puede ser transferido ADN entre bacterias de especies
diferentes?
Porqué lo que se requiere
para que se lleve correctamente la transferencia por transformación es que
exista homología entre el ADN de la bacteria donante y el ADN de la bacteria receptora, esto para que se pueda
llevar la recombinación adecuadamente.
Es decir, cualquier porción
del genoma de la célula donante puede incorporarse, siempre y cuando sea igual
o similar a la de la célula receptora. El DNA de la célula donante para que
pueda ser incorporado al cromosoma de la célula receptora y no tenga ningún
problema para ser incorporado debe tener las siguientes características: debe
ser de doble hélice, similar al DNA de la célula receptora, porque el ADN de la bacteria donadora que entra a la
bacteria receptora, se pega en la región que exista mayor homología entre las
bases, esto para que se lleve a cabo la recombinación del ADN, debe tener bajo
peso molecular y tamaño pequeño.
Con estas características la bacteria que las
presente, puede ser donadora para otras, sin necesidad de pertenecer a la misma
especie. Pueden ser de diferentes especies o cercanas.
Con estas recombinaciones se
ha logrado que numerosas bacterias sean inmunes a diferentes antibióticos y
como consecuencia se hacen más fuertes y logran transmitir esas características
a sus descendientes, cuando se dividen.
Existen varios géneros con
especies que poseen sistemas naturales de transformación:
Entre las bacterias Gram positivas los
ejemplos más estudiados son los de:
Streptococcus
Bacillus
Pero también se puede llevar acabo la transferencia
del ADN de forma artificial. Esto con la intervención del humano, llevando
acabo diferentes técnicas para hacer mejoramientos de organismos, utilizando diferentes
especies y entre diferentes especies. Recombinando el ADN de los organismos.
También porque muchas especies de bacterias carecen de sistemas naturales de
transformación.
BIBLIOGRAFIA